Раздвоение позвоночника у плода
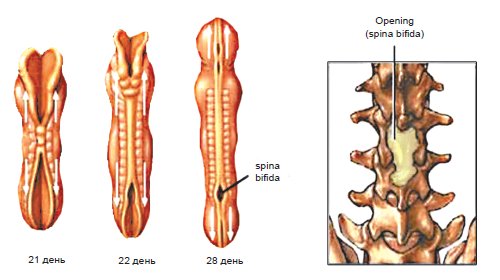
Расщепление позвоночника, незаращение дужки позвонка[1] (лат. Spina bifida, англ. split spine) — порок развития позвоночника, разновидность дефектов нервной трубки[en], часто сочетающийся с дефектами развития спинного мозга. Порок представляет собой неполное закрытие нервной трубки в не полностью сформированном спинном мозге.
Общая информация[править | править код]
Этот порок возникает на 3-й неделе беременности. Он представляет собой неполное закрытие нервной трубки в не полностью сформированном спинном мозге. Кроме того, позвонки над открытой частью спинного мозга сформированы не полностью.
При несмыкании пятого участка нервной трубки обнаруживается поддающийся коррекции врождённый порок — расщепление позвоночника, или spina bifida.
Из-за неполного закрытия нервной трубки (в недосформированном спинном мозге) у рождённого ребёнка позвоночные дужки над открытой частью спинного мозга (часто в поясничном отделе) отсутствуют либо деформированы, мозг торчит в виде грыжи.
Частота spina bifida колеблется от 1 до 2 на 1000 новорожденных. Частота повторных родов с этим пороком от 6 % до 8 %, что говорит о генетическом факторе развития заболевания. Более высока частота данной патологии у детей, родившихся от более пожилых матерей. Однако, несмотря на эти данные, 95 % новорожденных со spina bifida рождаются у родителей, у которых не было spina bifida. Такие факторы, как краснуха, грипп, тератогенные вещества, являются предрасполагающими.
В зависимости от тяжести расщепление позвоночника делят на несколько подтипов.
Spina bifida occulta[править | править код]
Часто эта форма называется «скрытое расщепление позвоночника», так как при этом спинной мозг и нервные корешки в норме, а также отсутствует дефект в области спины. Данная форма характеризуется лишь небольшим дефектом или щелью в позвонках, которые формируют позвоночный столб. Зачастую эта форма патологии настолько умеренно выражена, что не вызывает каких-либо беспокойств. При этом такие больные даже не знают о наличии у себя этого порока развития и узнают об этом лишь после рентгенографии. Чаще всего эта форма патологии возникает в пояснично-крестцовом отделе позвоночника. У 1 из 1000 больных могут отмечаться проблемы с функцией мочевого пузыря или кишечника, боли в спине, слабость мышц ног и сколиоз.
Менингоцеле[править | править код]
Возникает, когда кости позвоночника не закрывают спинной мозг полностью. При этом мозговые оболочки через имеющийся дефект выпячиваются в виде мешочка, содержащего жидкость. Этот мешочек состоит из трёх слоев: твёрдой мозговой оболочки, паутинной оболочки и мягкой мозговой оболочки. В большинстве случаев спинной мозг и нервные корешки нормальны либо с умеренным дефектом. Очень часто «мешочек» мозговых оболочек покрыт кожей. В этом состоянии может потребоваться хирургическое вмешательство.
Миеломенингоцеле (spina bifida cystica)[править | править код]
Эта наиболее тяжёлая форма составляет около 75 % всех форм расщепления позвоночника. Через дефект позвоночника выходит часть спинного мозга (так называемая мозговая грыжа). В некоторых случаях «мешочек» со спинным мозгом может быть покрыт кожей, в других случаях наружу могут выходить сама ткань мозга и нервные корешки. Степень неврологических нарушений напрямую связана с локализацией и тяжестью дефекта спинного мозга. При вовлечении в процесс конечного отдела спинного мозга могут отмечаться нарушения только мочевого пузыря и кишечника. Более тяжелые дефекты могут проявляться в виде параличей ног вместе с нарушением функции мочевого пузыря и кишечника.
Статистика[править | править код]
Частота встречаемости от 1 до 2 на 1000 новорождённых в мире.
Причины[править | править код]
Считается, что расщепление позвоночника вызвано сочетанием генетических и внешних факторов[2]. Если у родителей уже есть ребёнок с данной патологией или если она есть у одного из родителей, то вероятность рождения следующего ребёнка с расщеплением позвоночника повышается до 4 %[3]. Дефицит фолиевой кислоты во время беременности также играет значительную роль[2]. Другие факторы риска: противосудорожные препараты на основе вальпроевой кислоты (Депакин)[4], цитостатические препараты (антагонисты пуринов и антагонисты пиримидинов)[5]; ожирение и плохо управляемый диабет[3]. Частое употребление алкоголя вызывает макроцитоз, который разрушает фолиевую кислоту. После прекращения употребления алкоголя требуется месячный период времени для восстановления костного мозга от макроцитоза[5].
У европейцев или латиноамериканцев риск более высокий. Девочки более склонны к рождению с расщеплением позвоночника[4].
Определённые мутации в гене VANGL1 являются факторами риска развития расщепления позвоночника: эти мутации были связаны со spina bifida в некоторых семьях с историей расщепления позвоночника[6].
Лечение[править | править код]
Стандартным и общепринятым методом является лечение после родов[7]. Эта операция направлена на предотвращение дальнейшего повреждения нервной ткани и профилактику инфекций. Нейрохирурги стремятся закрыть дефект позвоночника: спинной мозг и его нервные корешки помещаются обратно в спинномозговой канал и покрываются мозговой оболочкой. Хирургическим путём может быть установлен шунт для обеспечения непрерывного слива избыточной спинномозговой жидкости, вырабатываемой в головном мозге, как это происходит при гидроцефалии. Шунты чаще всего стекают в брюшную или грудную полость[8].
Есть предварительные данные об эффективности[9] пренатального (то есть до родов) лечения, в то время как поражённый плод находится в матке[10]. По состоянию на 2014 год соотношение пользы и вреда от пренатальной хирургии плода при этой патологии остаётся сомнительным[7]. 40 % новорожденных, которых прооперировали внутриутробно, всё равно нуждались в установке шунта[10].
Лечение расщепления позвоночника во время беременности небезопасно: высок риск рубцевания матки и преждевременных родов[10].
Есть две формы пренатального лечения. Первая — это операция, при которой раскрывают матку через разрез и устраняют расщепление позвоночника. Вторая — через фетоскопию[8].
Профилактика[править | править код]
Так как точные причины расщепления позвоночника неизвестны, не существует какого-либо известного способа его надёжного предотвращения. Однако было показано, что употребление матерью фолиевой кислоты помогает снизить частоту возникновения этого порока у новорождённых. Источниками фолиевой кислоты являются цельные зёрна, обогащённые сухие завтраки, сушёные бобы, листовые овощи и фрукты[11].
Обогащение зерновых продуктов фолиевой кислотой рекомендуется в Соединённых Штатах с 1998 года. Управление США по контролю за продуктами и лекарствами и Агентство общественного здравоохранения Канады[12] рекомендовали планирующим забеременеть женщинам детородного возраста принимать по меньшей мере 0,4 мг фолиевой кислоты в день, начав не менее, чем за три месяца до зачатия, и продолжать приём в течение первых 12 недель беременности[13]. Женщины, которые уже родили ребёнка с расщеплённым позвоночником или другим типом дефекта нервной трубки, или принимают противосудорожное лекарство, должны принимать более высокую дозу: 4-5 мг в день[13].
В соответствии с приказом Министерства здравоохранения и социального развития РФ от 3 декабря 2007 г. № 736 «Об утверждении перечня медицинских показаний для искусственного прерывания беременности»[14], при выявлении у плода во время беременности врождённых аномалий (пороков развития), деформаций и хромосомных нарушений (коды по МКБ от Q00 до Q99) вопрос о прерывании беременности и неблагоприятном прогнозе для жизни плода должен решаться индивидуально перинатальным консилиумом врачей.
Примечания[править | править код]
- ↑ Аномалии развития позвоночника
- ↑ 1 2 What causes spina bifida? (англ.). National Institutes of Health (30 May 2012). Дата обращения: 13 марта 2017.
- ↑ 1 2 How many people are affected by or at risk for spina bifida? (англ.). National Institutes of Health (30 November 2012). Дата обращения: 13 марта 2017.
- ↑ 1 2 Spina bifida. Risk factors (англ.). Mayo Clinic (27 August 2014). Дата обращения: 13 марта 2017.
- ↑ 1 2 Vincent E Herrin. Macrocytosis. Risk factors (англ.). Medscape (24 September 2016). Дата обращения: 13 марта 2017.
- ↑ Kibar Z., Torban E., McDearmid J. R., Reynolds A., Berghout J., Mathieu M., Kirillova I., De Marco P., Merello E., Hayes J. M., Wallingford J. B., Drapeau P., Capra V., Gros P. Mutations in VANGL1 associated with neural-tube defects. (англ.) // The New England journal of medicine. — 2007. — Vol. 356, no. 14. — P. 1432—1437. — doi:10.1056/NEJMoa060651. — PMID 17409324.
- ↑ 1 2 Grivell R. M., Andersen C., Dodd J. M. Prenatal versus postnatal repair procedures for spina bifida for improving infant and maternal outcomes. (англ.) // The Cochrane database of systematic reviews. — 2014. — No. 10. — P. 008825. — doi:10.1002/14651858.CD008825.pub2. — PMID 25348498.
- ↑ 1 2 Joyeux L., Chalouhi G. E., Ville Y., Sapin E. Maternal-fetal surgery for spina bifida: future perspectives (фр.) // Journal de gynecologie, obstetrique et biologie de la reproduction. — 2014. — Vol. 43, no 6. — P. 443—454. — doi:10.1016/j.jgyn.2014.01.014. — PMID 24582882.
- ↑ Оперировать до рождения (рус.). Дата обращения 29 июня 2017.
- ↑ 1 2 3 Adzick N. S. Fetal surgery for spina bifida: past, present, future. (англ.) // Seminars in pediatric surgery. — 2013. — Vol. 22, no. 1. — P. 10—17. — doi:10.1053/j.sempedsurg.2012.10.003. — PMID 23395140.
- ↑ Folic acid fortification (англ.) (недоступная ссылка). U. S. Food and Drug Administration. Архивировано 18 сентября 2009 года.
- ↑ Folic Acid (англ.) (недоступная ссылка). Public Health Agency of Canada (16 December 2003). Архивировано 27 сентября 2006 года.
- ↑ 1 2 Why do I need folic acid? (англ.) (недоступная ссылка). HNS Direct (6 March 2006). Архивировано 13 апреля 2006 года.
- ↑ Приказ Министерства здравоохранения и социального развития РФ от 3 декабря 2007 г. № 736. «Об утверждении перечня медицинских показаний для искусственного прерывания беременности». garant.ru. Дата обращения: 13 марта 2017.
Ссылки[править | править код]
- Оперировать до рождения / В. Панюшкин
- Два мира / В. Панюшкин
- Мама ошиблась / В.Панюшкин
- Spina Bifida Overview / eMedicine MedScape, October 2014 (англ.)
Источник
Патологии позвоночника у плода встречаются в 1 случае на 1000 беременностей. Часто нарушения касаются не только самого позвоночного столба, но и спинного мозга. В основном плод с аномалией позвоночника гибнет внутриутробно или сразу после рождения, поэтому очень важно установить проблему как можно раньше, чтобы женщина обдуманно приняла решение о прерывании беременности.

Причины возникновения внутриутробных аномалий позвоночника
В большинстве случаев аномалия возникает в поясничном отделе, реже — в шейном, и совсем нечасто — в области крестца и грудном отделе.
Причины столь сложной патологии до сих пор не ясны. Но среди факторов, провоцирующих нарушение формирования спинного мозга, совершенно определенно можно выделить:
- TORCH-инфекцию;
- токсическое воздействие лекарств;
- сложные условия работы;
- употребление наркотиков и алкоголя;
- многолетний стаж курения.
Когда можно обнаружить патологии позвоночника у плода
Расщепление нервной трубки происходит в период с 19 по 30 день гестации (дня последней менструации у беременной). Аномалию позвоночника можно выявить уже на первом скрининге, который проводится на 11-й неделе беременности. Второй скрининг обычно подтверждает результаты 1-го скрининга и выявляет новые нарушения.
Миеломенингоцеле
75% всех случаев аномалий позвоночника у плода занимает миеломенингоцеле (spina bifida cystica). Патология выражается в выпячивании спинного мозга за пределы позвоночной дужки. Иногда мозговая ткань защищена кожей, но чаще выходит наружу вместе с нервными отростками. В последнем случае плод рождается с параличом нижних конечностей, проблемами с кишечником и мочевым пузырём. В 90% случаев у плода диагностируется гидроцефалия (водянка головного мозга).
Характерные признаки миеломенингоцеле на УЗИ:
- на задней поверхности позвоночника визуализируется жидкость;
- через позвоночную щели видно образование с жидкостью внутри;
- черепная ямка имеет меньшие размеры;
- ткани мозжечка смещены;
- выражено искривление позвоночника;
- размеры плода меньше нормы;
- диагностируется гидроцефалия из-за низкого расположения спинного мозга и блокировки спинномозговой жидкости.
При подозрении на патологию женщина сдаёт кровь на специфические ферменты. У неё повышен уровень альфа-фетопротеина, как и при других аномалиях плода. Затем беременную отправляют на 4D сканирование, во время которого можно увидеть объёмное изображение плода. Однако это становится возможным только с 20-й недели беременности.
Миеломенингоцеле — тяжёлая форма расщепления позвоночника, поэтому при подтверждении диагноза на УЗИ женщине рекомендуют сделать аборт. Даже если малыш родится живым, он не сможет ходить, у него будут проблемы с внутренними органами.
Операция по перемещению вышедшего за пределы позвоночного столба спинного мозга со спинномозговыми нервами проводится в течение 48 часов с момента рождения. Выпячивающаяся капсула помещается обратно в позвоночный канал, сверху нашиваются мышцы и кожа.
Такие дети нуждаются в особом лечении, которое существенно не улучшит их качество жизни. Очень низкий процент детей в будущем смогут ходить, но большинство будет нуждаться в инвалидной коляске, потому что нервные окончания повреждаются и не позволяют спинному мозгу нормально функционировать.
Синдром Клиппеля-Фейля
Синдром Клиппеля-Фейля встречается очень редко, в 1 случае из 120 000 беременностей, и имеет особенность передаваться по наследству.
Патология заключается в аномальном строении шейного отдела позвоночника, при котором позвонки сращиваются между собой. Шея практически отсутствует и, в зависимости от разновидности синдрома, патология имеет и другие нарушения. Наиболее опасна разновидность KFS3, при которой сращены не только шейные позвонки, но и грудные, а также поясничные. Из-за незаращения дужек позвоночника образуются дополнительные рёбра.
Помимо этого у плода визуализируются лишние пальцы, их недоразвитие или сращивание, гипоплазия почек, заращение мочеиспускательного канала, заболевания сердечно-сосудистой системы, отсутствует лёгкое, сбои в работе ЦНС. При любой форме синдрома у плода формируется искривление позвоночника (сколиоз).
Причина патологии — мутация гена GDF6. Выявляется аномалия не раньше 20-й недели беременности. При ультразвуковом исследовании на экране УЗИ заметно следующее:
- укорочение шеи;
- плод не поворачивает голову;
- низкая линия роста волос на затылке;
- асимметрия лица;
- отсутствие одного лёгкого;
- гипоплазия почки;
- срастание или недоразвитие пальцев на руке;
- лишние количество пальцев;
- сращение позвонков в различных отделах позвоночника.
Первые две разновидности синдрома Клиппеля-Фейля поддаются коррекции. Ребёнку проводят операцию, затем он проходит сложную восстановительную терапию. На сегодняшний день полностью восстановить позвоночник не удастся, однако человек сможет жить обычной жизнью, потому что умственные способности не затрагиваются.
При третьей форме патологии женщине предложат прерывать беременность, потому что при срастании позвонков ущемляются нервные корешки, из-за чего развиваются различные заболевания внутренних органов. Дети с формой KFS3 требуют особый уход за собой и всё-равно умирают в раннем возрасте.
Spina bifida
Spina bifida или неполное закрытие позвоночного канала, возникающее на ранних сроках беременности в связи с неправильным формированием нервной рубки. Помимо проблем с позвоночником, при Spina bifida имеется недоразвитие спинного мозга. 95% детей с такой патологией рождается у совершено здоровых молодых родителей.
Самой лёгкой формой патологии является Spina bifida occulta — небольшая щель в позвоночном столбе, не сопровождающаяся выпячиванием наружу спинного мозга и повреждением нервных корешков. Дефект внешне практически не заметен, и со стороны сложно сказать, что есть какая-то проблема.
Иногда у новорождённого наблюдаются проблемы с кишечником и мочевым пузырём, имеется сколиоз и слабый тонус ног. Единственным способом диагностики патологии является рентгенография. На скрининговом УЗИ она практически не видна, только при 4D УЗИ можно увидеть неполное сращение дужек позвоночного столба на поздних сроках беременности. Аномалия не требует коррекции, и прерывать беременность женщине не надо.
Кистозная гигрома шеи
Гигрома на шее у плода (лимфангиома) — это доброкачественная опухоль, которая образуется в результате нарушения формирования лимфасистемы в области шейных позвонков в период эмбрионального развития. Если нарушается лимфаток в месте соединения яремного мешка с яремной веной, образуется киста или несколько кист, заполненных фиброзно-серозной жидкостью. Опухоль локализуется возле шейных позвонков, влияя на развитии плода.
Патологию на УЗИ можно увидеть уже на 1-м скрининге на срок 11-12 недель. Главным показателем будет увеличение толщины воротникового пространства. Гигрома шеи у плода возникает как в результате хромосомных нарушений, так и под влиянием внешних причин — механической внутриутробной травмы, курение и употребление алкоголя матерью, перенесённые во время беременности инфекции.
На 2-м скрининге гигрома визуализируется как ассиметричное новообразование с плотной оболочкой, иногда имеющее перегородки внутри, расположенное в проекции шейного отдела позвоночника. Сама по себе опухоль не представляет угрозы для жизни плода.
На ранних сроках делается биопсия хориона с целью выявления хромосомных нарушений. Если они подтвердятся, женщине предложат прервать беременность. В случае отсутствия генетических отклонений врачи придерживаются выжидательной позиции. очень часто к 18-20 неделе беременности гигрома рассасывается сама собой.
Если этого не произойдёт, то у малыша после рождения вероятно наличие следующих отклонений:
- парез лицевого нерва — обездвиживание мускулатуры лица по причине длительного сдавливания гигромой нервного волокна;
- деформация позвоночника (чаще всего встречается кривошея — искривление шейного отдела из-за воспалительного процесса в шейных мышцах вследствие перенапряжения постоянного давления опухоли);
- деформация затылочной кости и челюсти;
- нарушение глотательной функции;
- обструкция дыхательных путей (непроходимость дыхательного канала из-за перекрытия трахеи гигромой).
Лечится гигрома консервативно после рождения ребёнка. Если причиной патологии не являются хромосомные нарушения, прогноз для малыша благоприятен.
Выводы
Чтобы исключить любые патологии позвоночника у плода, нужно уже на ранних сроках проходить скрининг с помощью хорошего УЗИ-аппарата. Аномалии позвоночника видны даже при первом обследовании, что позволяет, в случае тяжелых нарушений, своевременно прервать беременность.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter
Поделиться ссылкой:
Источник
Spina bifida — дефект развития нервной трубки, представляющий собой расщепление спинномозгового канала (спинальный дизрафизм), часто с формированием грыж спинного мозга.
Центральная нервная система формируется из эктодермы на 3-й неделе эмбрионального развития. Длина эмбриона в этот период составляет всего 15 мм. Листки эктодермы сближаются и формируют невральный желобок, а затем, сблизившись, нервную трубку (рис. 1). Вокруг формируется костное кольцо. В норме закрытие невральной трубки происходит к 28-му дню гестации. Однако при нарушениях закрытия формируются такие ее дефекты, как анэнцефалия, энцефалоцеле и spina bifida (рис. 2).
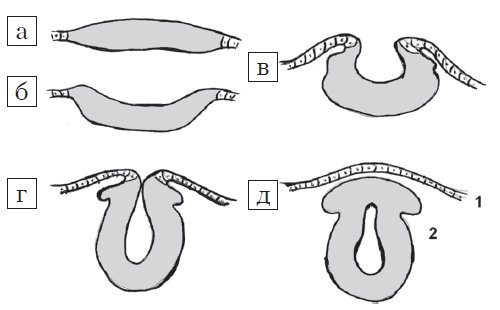
Рис. 1. Стадии эмбриогенеза нервной трубки: поперечный схематических разрез.
а) Медуллярная пластинка.
б, в) Медуллярная бороздк.
г, д) Нервная трубка: 1 — роговой листок (эпидермис); 2 — нейральные гребни.

Рис. 2. Формирование дефекта нервной трубки.
Типичным для всех видов и форм спинальных дизрафий является их заднее расположение с дефектом заднего полукольца позвоночного канала. Крайне редко (менее 1% случаев) незаращение формируется на переднебоковой поверхности канала, и возникают передние спинномозговые грыжи.
Передняя и задняя расщелины позвонка могут проходить по срединной линии, а также располагаться асимметрично. В ряде случаев щель располагается косо. Если расщепление позвонков происходит по срединной линии, то деформация позвоночника может быть незначительной или вовсе не выражена. Однако при асимметричном и косом расположении щели в сочетании с другими аномалиями развития позвонков (например, односторонней микроспондилией половины позвонка, аномалией суставных отростков) развивается выраженная деформация позвоночника.
Наиболее часто (до 70% случаев) spina bifida локализуется в пояснично-крестцовой области, в 21% — в грудном отделе и в 9% — прочей локализации [1].
Выделяют три варианта spina bifida
- Spina bifida occulta. Этот вариант еще называют «скрытым», так как видимого наружного дефекта нет. Скрытые незаращения позвоночника обычно локализуются в пояснично-крестцовой области и, как правило, клинически ничем не проявляются. Часто они являются случайной «находкой» при рентгенологическом исследовании позвоночника или МРТ. Анатомическая сущность скрытой расщелины позвоночника состоит в неполном заращении дужки позвонка. Это наиболее благоприятный вариант spina bifida. Иногда в области дефекта имеются «маркеры» или кожные стигмы в виде липом, кистозных и/или солидных масс, участков аномального оволосения, гиперпигментации. При закрытых дефектах также встречаются аномалии позвонков, деформации стоп и аномально низкорасположенный конус. Закрытый вариант spina bifida не сопровождается синдромом Арнольда Киари II, вентрикуломегалией и другими интракраниальными изменениями [2].
- Meningocele. Менингоцеле представляет собой расщепление позвоночника с выпячиванием в дефект твердой мозговой оболочки, но без вовлечения в процесс нервных структур (рис. 3). Содержимое грыжевого мешка — мозговые оболочки и ликвор, форма его — обычно стебельчатая с суженной ножкой. Костный дефект захватывает обычно два-три позвонка. Клинические проявления заболевания вариабельны и колеблются от бессимптомного течения до нарушения функции тазовых органов, двигательных и чувствительных расстройств. Данный вариант spina bifida встречается редко.
- Myelomeningocele. Это наиболее тяжелая форма spina bifida, с вовлечением в грыжевой мешок оболочек, спинного мозга и его корешков. Костный дефект обычно широкий и протяженный, захватывает от 3 до 6-8 позвонков. Степень неврологического дефекта всегда тяжелая параплегия нижних конечностей, чувствительные расстройства, нейрогенный мочевой пузырь и парез кишечника. Именно эта форма спинномозговых грыж встречается наиболее часто — около 75% всех форм [3-5]. Почти во всех случаях миеломенингоцеле сочетается с синдромом Арнольда — Киари II. Таким образом, обнаружение признаков аномалии Арнольда — Киари II у плода является маркером наличия spina bifida. Кроме того, в 70-80% случаев у плода развивается гидроцефалия [5, 6].
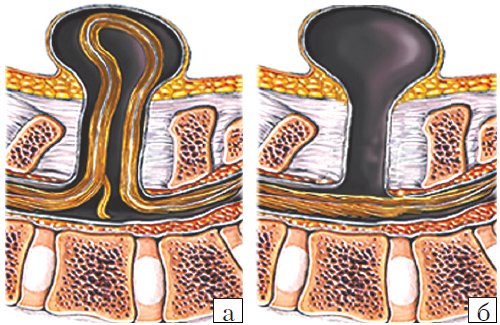
Рис. 3. Схема дефектов позвоночника плода.
а) Meningomyelocele.
б) Meningocele.
Представляем клинические наблюдения, демонстрирующие возможности эхографии в диагностике дефектов позвоночника плода.
Клиническое наблюдение 1
Пациентка К., 26 лет, обратилась в клинику в 23 нед беременности. Беременность первая. Исследование проводилось на аппарате Accuvix-XQ (Samsung Medison) с использованием режима поверхностной объемной реконструкции 3D/4D. Показатели фетометрии полностью соответствовали сроку беременности. В процессе сканирования позвоночника во фронтальной и сагиттальной плоскостях выявлена угловая деформация позвоночника в грудном отделе, протяженностью около трех позвонков. В поперечной плоскости сканирования нарушения структур и целостности тканей не было обнаружено. В режиме 3D/4D реконструкции было выявлено асимметричное расхождение ребер правой и левой стороны грудной клетки (рис. 4).
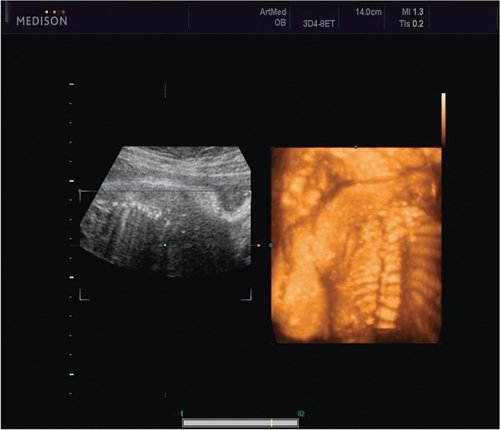
Рис. 4. Эхографическая картина асимметрии ребер в режиме 3D реконструкции.
Ребра левой стороны были сближены, межреберные промежутки уменьшены по сравнению с противоположной стороной (рис. 5, 6). Другой патологии у плода не было выявлено. Заподозрен врожденный сколиоз, основой которого является наличие боковых полупозвонков (hemivertebrae) или боковых клиновидных позвонков. В 26 нед ультразвуковая картина сохранялась. При проведении трехмерной эхографии получено отчетливое изображение асимметрии реберных дуг и сколиотическая деформация позвоночника.
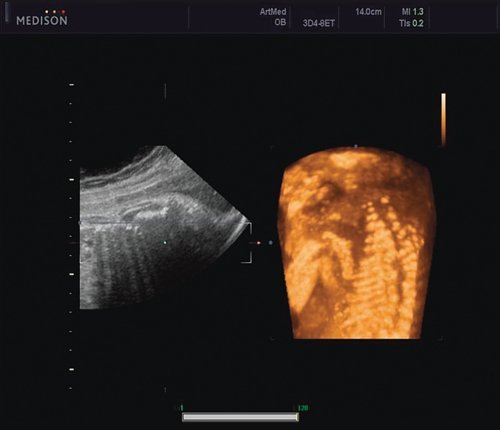
Рис. 5. Асимметрия межреберных промежутков в режиме 3D реконструкции.
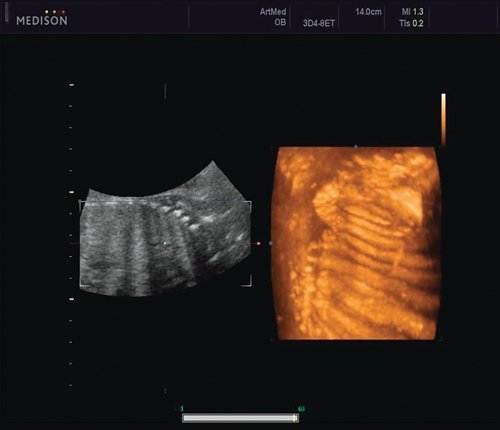
Рис. 6. Асимметрия межреберных промежутков в режиме 3D реконструкции.
В 30 нед фетометрические показатели плода соответствовали сроку беременности. Сколиотическая деформация позвоночника сохранялась. Дополнительно выявлена оболочечная грыжа, исходящая из грудного отдела позвоночника, в области деформированных позвонков. Грыжа представляла собой стебельчатой формы образование с суженной ножкой (рис. 7, 8). Концевая часть ее была расширена в виде петли и заполнена анэхогенным содержимым (ликвором), которое отчетливо дифференцировалось на фоне «мутных» околоплодных вод (рис. 9). Таким образом, диагноз был уточнен: spina bifida — менингоцеле.
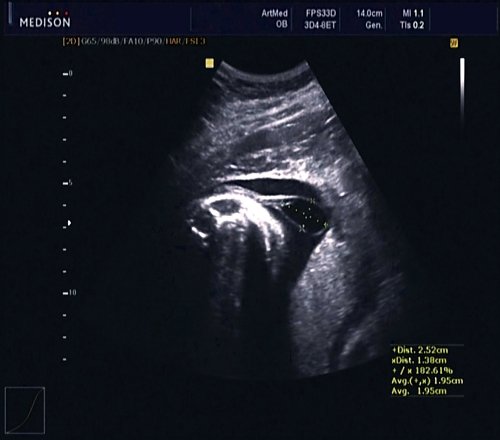
Рис. 7. Беременность 30 нед. Стебельчатая форма менингоцеле.
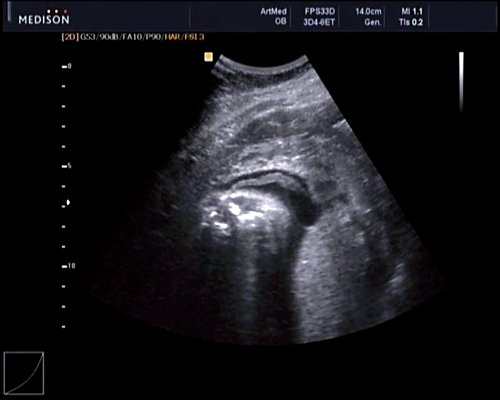
Рис. 8. Место выхода мозговой оболочки.
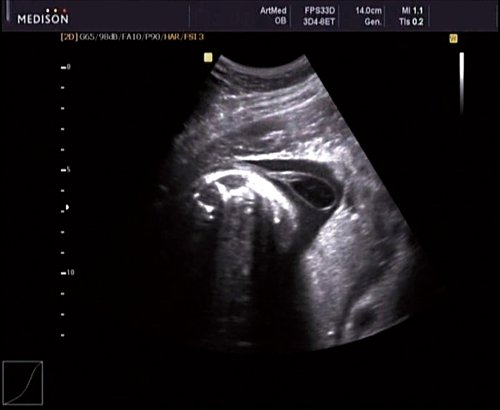
Рис. 9. Беременность 30 нед. Эхогенность ликвора ниже эхогенности околоплодных вод.
Дальнейшее наблюдение не выявило значительной динамики обнаруженных изменений.
После рождения диагноз spina bifida — менингоцеле подтвержден. Ребенок успешно оперирован, у него отсутствуют какие-либо неврологические расстройства.
В данном случае, локальная угловая деформация позвоночника в грудном отделе и асимметрия ребер явились начальными ультразвуковыми признаками открытой формы spina bifida — менингоцеле во II триместре беременности. Манифестация грыжи возникла только в III триместре.
Клиническое наблюдение 2
Беременная М., 21 года. Впервые обратилась в клинику в срок 20 нед беременности. Исследование проводилось на аппарате SonoAce-R7 (Samsung Medison) с использованием режима поверхностной объемной реконструкции 3D/4D. При изучении позвоночника плода в трех плоскостях костных деформаций не выявлено. В грудном отделе позвоночника обнаружено тонкостенное кистозное образование с анэхогенным содержимым, стебельчатой формы (рис. 10-12). Степень «прозрачности» содержимого была выше околоплодных вод, что позволяло идентифицировать его как ликвор. В проекции грыжевого выпячивания располагалась петля пуповины, дифференциальную диагностику которой без труда удалось провести с помощью ЦДК (рис. 13).
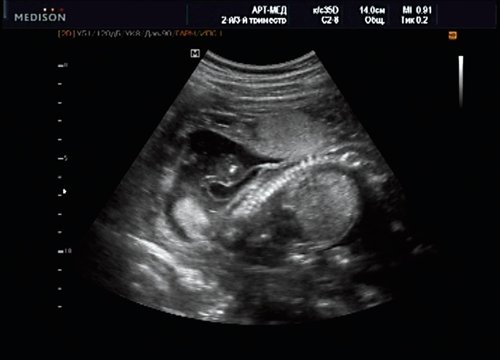
Рис. 10. Беременность 20 нед. Менингоцеле: типичное кистозное образование стебельчатой формы.
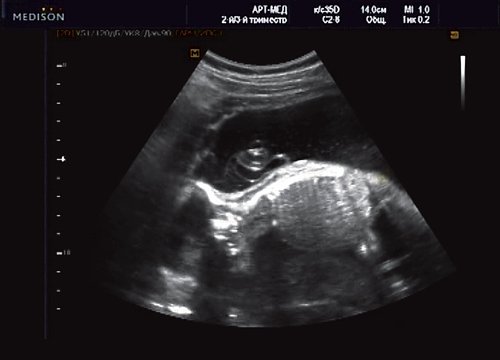
Рис. 11. Беременность 20 нед. Менингоцеле.
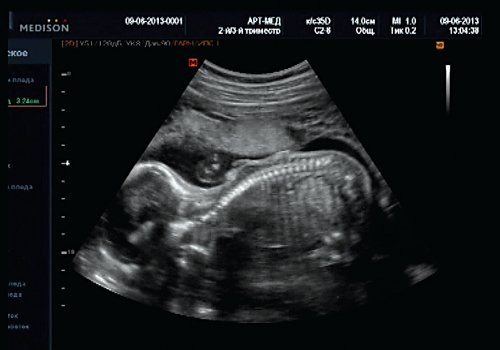
Рис. 12. Менингоцеле. В сагиттальном срезе видна неровность кожи в проекции расщелины.
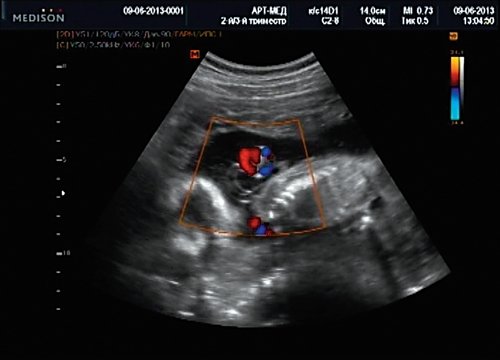
Рис. 13. Петля пуповины в режиме ЦДК.
У плода наблюдалась выраженная гидроцефалия, обусловленная синдромом Аронольда — Киари II (рис. 14, 15).
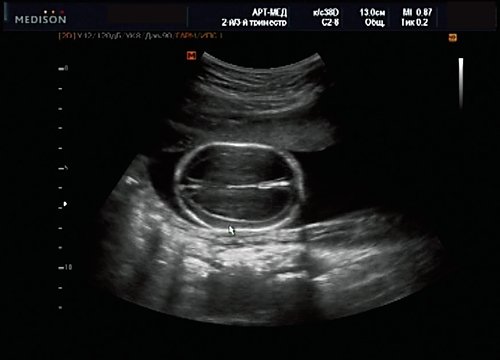
Рис. 14. Беременность 20 нед. Гидроцефалия.
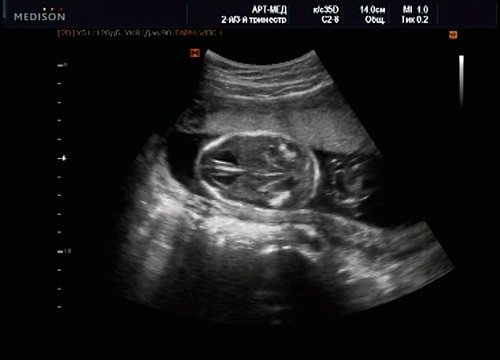
Рис. 15. Беременность 20 нед. Удлинение ножек мозга и вклинение мозжечка в затылочное отверстие при синдроме Арнольда — Киари II.
Учитывая типичную форму грыжевого выпячивания и отсутствие элементов нервной ткани, было высказано предположение о наличии у плода менингоцеле (рис. 16). Женщина приняла решение о прерывании беременности.
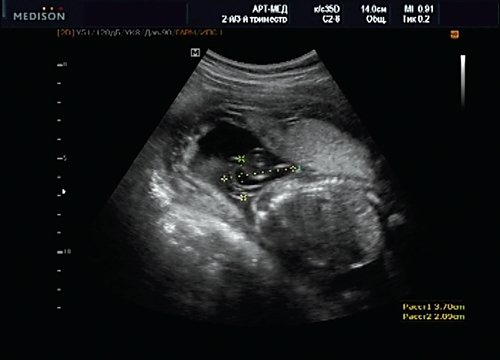
Рис. 16. Беременность 20 нед. Менингоцеле размером 37х21 мм.
Клиническое наблюдение 3
Беременная 27 лет, обратилась в клинику в 18 нед. При эхографии обнаружен синдром Арнольда — Киари II, умеренно выраженная гидроцефалия (рис. 17).
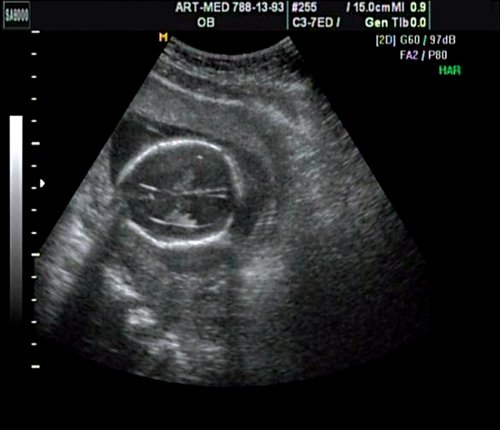
Рис. 17. Беременность 18 нед. Гидроцефалия.
В крестцовом отделе позвоночника выявлена spina bifida cysticа (рис. 18).
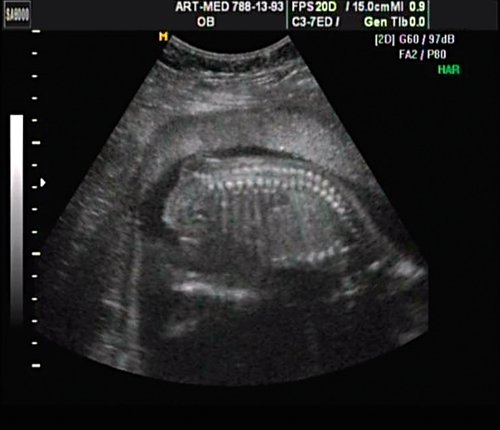
Рис. 18. Беременность 18 нед. Spina bifida в крестцовом отделе.
Женщиной принято решение о прерывании беременности.
Клиническое наблюдение 4
Беременная 25 лет, обратилась в клинику в срок 18 нед. При эхографии выявлена грубая кифотическая деформация позвоночника в поясничном отделе (рис. 19).
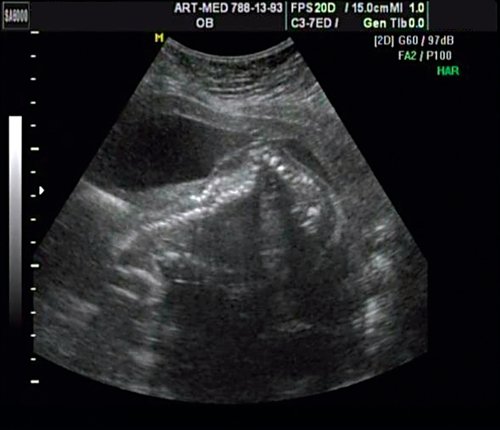
Рис. 19. Деформация позвоночника.
В проекции деформации определяется миеломенингоцеле (рис. 20).
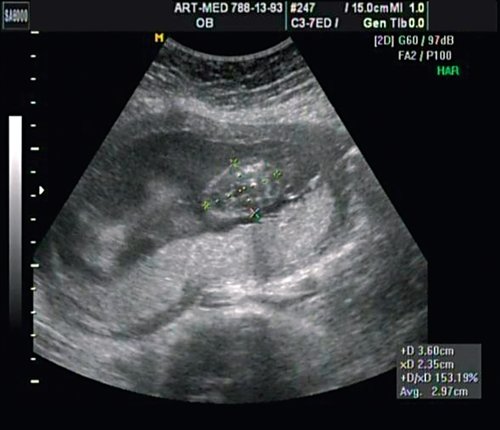
Рис. 20. Миеломенингоцеле.
Обнаружение типичных эхографических признаков позволило установить диагноз миеломенингоцеле.
Женщиной принято решение о прерывании беременности.
Заключение
Диагностика открытых форм spina bifida не является трудной задачей во II триместре беременности. Обнаружение таких изменений, как синдром Арнольда — Киари II и дефект позвоночника с формированием грыжевого выпячивания не оставляют сомнений в диагнозе. Исключение составляют лишь те случаи, когда ультразвуковая манифестация порока представлена только деформацией позвоночника. В настоящее время наибольший интерес представляет выявление данного порока в I триместре беременности. Изучаются такие ультразвуковые критерии, как отсутствие интракраниальной «прозрачности» (intracranial translucency), сглаженность угла ствола мозга, уменьшение бипариетального размера ниже 5-го процентиля и т.д. Таким образом, диагностика spina bifida остается важной задачей пренатальной диагностики.
Литература
- Amari F., Junkers W., Djalali S., Hartge D.R. et al. Fetal spina bifida — prenatal course and outcome in 103 cases // J. Ultrasound in Obstetrics & Gynecology. 2009. N 34. P. 82.
- Pugash D., Irwin B., Lim K., Thiessen P., Poskitt K., Cochrane D. Prenatal diagnosis of closed spinal dysraphism // J Ultrasound in Obstetrics & Gynecology. 2006. N 28. P. 547.
- Tortori-Donati P., Rossi A., Cama A. Spinal dys-raphism: a review of neuroradiological features with embryological correlations and proposal for a new classification // Neuroradiology. 2000. N 42. P. 471-491.
- Van den Hof M.C., Nicolaides K.H., Campbell J., Campbell S. Evaluation of the lemon and banana signs in one hundred thirty fetuses with open spina bifida // Am J Obstet Gynecol. 1990. N 162. P. 322-327.
- Ghi T., Pilu G., Falco P., Segata M., Carletti A., Cocchi G., Santini D., Bonasoni P., Tani G., Rizzo N. Prenatal diagnosis of open and closed spina bifida.Ultrasound Obstet Gynecol. 2006. N. 28. P. 899-903.
- D’Addario V., Rossi A.C., Pinto V., Pintucci A., Di Cagno L. Comparison of six sonographic signs in the prenatal diagnosis of spina bifida // J Perinat Med. 2008. N 36. P. 330-334.
